Introducción.
Cryptosporidium, aún conocido como coccidio, con Cyclospora y Cystoisospora, pertenece al grupo de los Gregarinos, en el phylum Apicomplexa. Los gregarinos son un grupo diverso de parásitos que infectan principalmente el intestino y otros espacios extracelulares. Estos tres coccidios (nomenclatura tradicional) se caracterizan por la eliminación de ooquistes con la materia fecal de los hospederos. Ademas, las fases infectantes se desplazan mediante movimientos de deslizamiento (Francia et al., 2016).
Cryptosporidium es un parásito epicelular, monoxeno, con varias especies. Es un patógeno emergente e importante agente etiológico no viral de diarrea en humanos y animales a nivel mundial.
Los grupos específicos con mayor riesgo de adquirir la parasitosis son niños, individuos desnutridos, pacientes con algún tipo de inmunocompromiso, humoral o celular (SIDA, entre otros); también es una causa de importante de «diarrea del viajero» y de brotes epidémicos.
El protozoo fue descubierto en ratones por Tizzer (1907); a raíz de ese hallazgo fué reportado en un amplio rango de animales vertebrados, domésticos y silvestres, muchos de ellos neonatos. Su importancia como patógeno humano se reconoció en 1976, cuando se diagnosticó en 2 pacientes con diarrea acuosa. A partir de entonces, se identificó con mayor frecuencia, particularmente en sujetos inmunodeprimidos y en brotes epidémicos por ingesta de agua contaminada (esta forma de diseminación cobró relevancia después del brote detectado en Milwaukee, EUA, con 403 000 casos detectados). La infección crónica ha sido relacionada principalmente con el síndrome de inmunodeficiencia adquirida, pero las infecciones en sujetos inmunocompetentes han aumentado de manera muy importante. Actualmente, se consideran <8 millones de casos/año (Una Ryan et al., 2018).
Tanto Giardia duodenalis como Cryptosporidium spp. fueron incluidos dentro de la iniciativa de «enfermedades tropicales menospreciadas» (Neglected Tropical Diseases – NTD) de la OMS, desde 2004.
Morfología. Clasificación.
Se reconocen arededor de 20 diferentes especies de Cryptosporidium que causan infecciones moderadas o severas en humanos pero los principales agentes causales son Cryptosporidium hominis y Cryptosporidium parvum, con base en datos morfológicos, biológicos y moleculares (Ryan et al, 2014; Vitaliano et al., 2015; Moore et al., 2016; Khan et al., 2017) y se han identificado alrededor de 61 genotipos de especie incierta, con base en la secuencias de ssrRNA. La utilización de herramientas moleculares para el análisis genético, pruebas con PCR y el estudio de los microsatélites han confirmado la autenticidad de especies y la existencia de genotipos dentro de ellas. La taxonomía de este organismo está en rápida evolución; así, por ejemplo, Cryptosporidium pestis, antes el genotipo C. parvum, ha sido aceptado, de acuerdo al International Code of Zoological Nomenclature (Chalmers et al., 2010; Fayer. 2010; Šlapeta. 2011; Xiao et al., 2012). La revisión más reciente enlista 30 especies y un número en aumento de genotipos (Thompson et al., 2016).
La enfermedad en el humano se atribuye con mayor frecuencia a 8 de dichas especies, aunque existen reportes incidentales de infección por otros criptosporidios (Chalmers, et al. 2010).
Especies de Cryptosporidium más frecuentes en el humano |
|
Cryptosporidium hominis |
Humano |
C. parvum |
Ganado, humano |
C. andersoni |
Ganado, camellos |
C. felis |
Gatos |
C. canis |
Perros |
C. suis |
Cerdos |
C. muris |
Roedores |
C. meleagridis |
Aves |
Modificado de: Chalmer RM, Davies AP. Clinical cryptosporidiosis. Ex. Parasitol, Jan 2010. |
|
La mayoría de los ooquistes, esféricos o elípticos, miden entre 4 – 6 µm y las características morfológicas ayudan poco en la diferenciación de especies; se requiere de morfometría, técnicas moleculares y el conocimiento de especificidad de hospedero para la identificación correcta.
Ciclo biológico. Transmisión.
La transmisión es fecal-oral, por contacto directo de hospedador-hospedador y a través de agua o alimentos contaminados con ooquistes, infectantes en el momento de ser eliminados con la materia fecal del hospedero. Cabe mencionar que la criptosporidiosis se ha identificado en brotes epidémicos debidos a contaminación de redes de agua potable, de superficie y recreativas.
En un estudio realizado en Alejandría, Egipto, se encontró que más del 56% de los billetes y monedas estaban contaminados conCryptosporidium (Una Ryan et al., 2018).
En países desarrollados, la parasitosis se presenta principalmente en la forma de brotes epidémicos debidos a fuentes de agua o alimentos contaminados.
Se reconoce que a pesar del lavado cuidadoso de frutas y hortalizas de hoja verde, los ooquistes, debido a su cubierta y por tanto, su resistencia, pueden encontrarse en el estoma de dichas frutos. Los ooquistes de Cryptosporidium permanecen viables en agua de mar durante 1 año. También se ha documentado su concentración en moluscos bivalvos y existe evidencia creciente de que el parásito puede multiplicarse en ambientes libres de hospederos (Thompson et al., 2016).
Los ooquistes de Cryptosporidium, con pared doble y 4 esporozoítos desnudos en su interior, sobreviven en el ambiente por largos periodos de tiempo (entre 20 – 30 °C, durante semanas/meses). Una vez en tracto digestivo, principalmente a nivel de intestino delgado, los esporozoítos (forma invasiva) son liberados a través de una ranura en los ooquistes en disolución.

Esquema. Morfología general.Modficado de: BIODIDAC
Los esporozoítos poseen un complejo apical, auxiliar en la adhesión a la membrana celular del hospedero, que envuelve las formas invasivas del parásito y da lugar a una vacuola parasitófora. Esta vacuola, que engloba al esporozoíto en un nicho protector especial extracitoplásmico (epicelular), presenta una región electrodensa en la base, denominada organelo de alimentación o epimerita

Ciclo biológico de Cryptosporidium. Transmisión, forma infectante. Fuente: PHIL 3386 – CDC/Alexander J. da Silva, PhD/Melanie Moser

Ciclo biológico de Cryptosporidium. En tracto gastrointestinal. Fuente: PHIL 3386 – CDC/Alexander J. da Silva, PhD/Melanie Moser
El desarrollo ulterior comprende la transformación del esporozoíto en trofozoíto y la reproducción de manera asexual, pormerogonia (la división celular es por endopoligenia: formación de células hijas por gemación), que da lugar a merontes de dos tipos: merontes I con 8 merozoítos, que invaden otras células, con repetición del ciclo y formación de otros merontes I, o merontes II, con 4 merozoítos; estos últimos dan origen a estadios sexuales y la reproducción sexual ocurre por gametogonia, con micro y macrogametos. Los cigotos resultantes pasan por una última fase de desarrollo ( esporogonia), que culmina con la producción de ooquistes; Cryptosporidium presenta dos tipos funcionales de ooquistes: a) infectantes, de pared gruesa, con 4 esporozoítos desnudos (sin esporoquiste) – eliminados con las heces; b) ooquistes de pared delgada, involucrados en la auto-infección intestinal (Grinberg & Widmer. 2016).
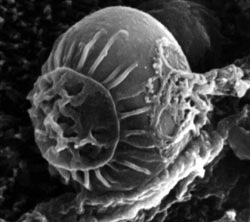
SEM. Cryptosporidium sp. Organelo de alimentación expuesto (epimerita). S.J. Upton, Kansas University

Cryptosporidium sp. en células epiteliales de vesícula. CDC/Dr. E. Ewing Jr
Las 3 fases de reproducción abarcan unas 12 – 24 h, con una nueva generación de parásitos y formas autoinfectantes en cada ocasión. Ante tal número de organismos no es de extrañar que en sujetos inmunocomprometidos las formas parasitarias puedan extenderse hasta conductos biliares y pancreáticos, estómago y tracto respiratorio.
La autoinfección interna e infección crónica se explican por la sucesión de ciclos esquizogónicos y la presencia de ooquistes de pared delgada; la duración de la infección depende de varios factores, los más importantes asociados a la inmunocompetencia, edad y nutrición de los hospederos.
Cabe mencionar que existe evidencia en aumento de que el gregarino Cryptosporidium puede desenquistarse y multiplicarse sin la necesidad de encapsulación por las células hospederas y desarrollo epicelular (Grinberg & Widmer. 2016).
Espectro clínico.
Se contemplan:
– Estado de portador, asintomático.
– La enfermedad en sujetos inmunocompetentes, autolimitada, con duración entre 2 – 14 días, aunque puede prolongarse hasta 1 mes. Incluye diarrea acuosa , que puede ser de tipo coleriforme, ocasionalmente explosiva y fétida, dolor abdominal, flatulencia, vómito, anorexia, pérdida de peso.
– En menores de 2 años es más frecuente un cuadro severo, que incluye evacuaciones acuosas, ocasionalmente con moco, sin sangre, con deshidratación y desequilibrio electrolítico. Se ha asociado también a retardo en el crecimiento.
– La parasitosis en personas con algún tipo de inmunocompromiso, con diarrea de tipo coleriforme, puede representar la pérdida de varios litros (se han mencionado casos extremos con hasta 25 litros/24 h). Es una enfermedad asociada con frecuencia a pacientes con SIDA, quienes pueden presentar diarrea crónica de manera intermitente, con episodios hasta de 30 días y recurrencias. El desequilibrio hidroelectrolítico puede ser muy importante. Desarrollan sobre todo la parasitosis fulminante aquellos sujetos con cuentas de linfocitos CD4 menores a 50-100/µL con un síndrome de malabsorción más importante. La enfermedad extraintestinal (vesícula biliar, tracto respiratorio, hígado, páncreas) conlleva morbilidad y mortalidad mayores. Se ha reportado una mortalidad de aproximadamente el 50% en los 6 meses posteriores al inicio de la infección en estos sujetos.
Cualquiera de los cuadros asociado a signos y síntomas puede ser causa de malabsorción intestinal.
Respuesta inmune y Patogenia.
-
Es importante explicar los mecanismos que dan lugar a la diarrea osmótica, inflamatoria y secretora que se presenta en esta enfermedad, particularmente en sujetos inmunodeprimidos; sin embargo, hacen falta estudios. Se considera que el origen es multifactorial: están involucrados tanto el parásito como sus productos, la respuesta inmune del hospedero, que dan lugar a deficiencias en la absorción a nivel de intestino delgado y aumento en la secreción.
-
Adhesión. Entre otros factores se contemplan lectinas y glucoproteínas semejantes a la mucina, receptores de adherencia del esporozoíto.
-
Las células T, principalmente los linfocitos CD4+ son fundamentales en la respuesta inmune contra los criptosporidios, y al mismo tiempo, la atrofia de vellosidades y la hiperplasia de las criptas son cambios patológicos asociados a las células T. (Chalmers et al. 2010).
-
Apoptosis. La cascada de señales pro-apoptosis predominan a las 24 – 48 horas postinfección. Estudios in vitro.
-
Daño celular – Producido por el parásito. Productos del esporozoíto están involucrados en la desorganización de las uniones celulares, pérdida de la función de barrera, liberación de lactato-dehidrogenasa e incremento en la muerte celular. Fosfolipasas, proteasas, son moléculas que potencialmente pueden causar el daño tisular. (Borowski et al. 2008; Ortega-Pierres et al. 2009; Stark et al. 2010).
Histopatología.
Los cambios histopatológicos asociados a este organismo incluyen: diferentes grados de atrofia de las microvellosidades, edema de la submucosa, infiltrado inflamatorio mononuclear e hiperplasia de las criptas. Los estadios del parásito se observan en la zona apical de la membrana del enterocito.
Diagnóstico.
Es importante el diagnóstico diferencial con patologías causadas por Cyclospora e Cystoisospora, y otros patógenos intestinales que producen cuadros clínicos similares.

Cryptosporidium sp. Ooquistes. Examen en fresco

Tinción ácido alcohol. Chiang Mai University, Thailand y CDC.
Los ooquistes se recobran en materia fecal. Cuando se sospecha compromiso extraintestinal, es prudente buscarlos en bilis o esputo. La recuperación rutinaria se realiza por técnicas de concentración/flotación, entre ellas la técnica de Sheather (con sacarosa a una densidad de 1.27), el posterior extendido y tinción ácida mediante los métodos de Kinyoun en frío o caliente o Ziehl-Neelsen modificado (con ambos se obtienen ooquistes teñidos de color rojo).
Otra tinción de utilidad en los sitios donde se encuentra disponible es Acrifluor, que tiñe bien coccidios intestinales y micobacterias. No se puede diferenciar mediante microscopía los ooquistes de C. hominis, especies zoonóticas, y la diversidad de especies y genotipos. Únicamente los ooquistes de C. andersoni y C. muris pueden identificarse debido a su tamaño. (Thompson et al., 2016).
La observación de la muestra con microscopía de contraste de fase permite observar los ooquistes como cuerpos birrefringentes con uno o varios gránulos oscuros.
El material histológico obtenido por biopsia o durante necropsias, previa fijación, se tiñe con hematoxilina-eosina o Giemsa, dadas las características basófilas de los estadios de desarrollo de Cryptosporidium. Esta técnica se utiliza principalmente en estudios patológicos.
En algunos lugares se efectúa la filtración de grandes volúmenes de agua con filtros de policarbonato con poros menores a 1 µm para la obtención y marcaje posterior de ooquistes.

Cryptosporidium sp. Ooquistes infectantes. Contraste de fase. CDC

IFA. Quistes Giardia y ooquistes Cryptosporidium. CDC
También se utilizan kits (ELISA) para la identificación de coproantígenos e inmunofluorescencia (IFA).
Se han desarrollado diferentes técnicas de PCR para la detección y diferenciación de Cryptosporidium spp. a nivel de especie/genotipo y subtipos.
Se ha descrito el empleo de PCR en una plataforma robótica, para la identificación simultánea de Cryptosporidium spp. y otros patógenos concomitantes en materia fecal. (Fletcher et al., 2012). Actualmente, el gen utilizado con más frecuencia en la caracterización es SSU-rDNA. Gracias a investigaciones epidemiológicas moleculares, se han identificado genes adicionales que son herramientas de valor en la genotipificación de Cryptosporidium, entre ellos la proteína de choque térmico 70 kDA (HSP70) y la proteína de pared del ooquiste de Cryptosporidium (Thompson et al., 2016).

C. parvum . Técnica DIC. EPA, EEUU

C. parvum . Técnica DAPI (tinción vital que se basa en la absorción de fluorocromos específicos). EPA, EEUU.

Ooquistes de Cryptosporidium parvum y quistes de Giardia lamblia . Microscopia confocal. Lindquist HDA, EPA, EEUU.
Epidemiología.
El impacto global de las enfermedades diarreicas se estima en unos 62 millones de años de vida ajustados por discapacidad (DALYs). Aunque el peso de los diferentes patógenos que contribuyen a esta cifra es difícil de evaluar, la criptosporidiosis se considera una de las causas más frecuentes de diarrea en países que cuentan con datos epidemiológicos confiables.
(Karanis et al., 2007).
La criptosporidiosis es una enfermedad cosmopolita, con mayor en zonas con clima tropical o templado, que se presenta con frecuencia en pacientes con SIDA. En países en desarrollo, en los que prevalece una sanidad deficiente y hacinamiento, es más frecuente la transmisión oral-fecal, directa o indirecta, con brotes a nivel familiar o institucional, sin olvidar factores significativos como la ingesta de agua no potable y las zoonosis.
La prevalencia de la enfermedad en países industrializados oscila entre 0.1 y 27.1%, con una media de 4.9%, mientras que en países en desarrollo los resultados varían entre 0.1 a 31.5% con una media de 7.9%, excluyendo los brotes epidémicos específicos y a los sujetos con SIDA. Aún cuando los estudios epidemiológicos han demostrado que la parasitosis está más difundida de lo que anteriormente se pensaba, es difícil determinar la extensión del problema, tanto a nivel veterinario como médico.
En países con mayor desarrollo, la parasitosis se presenta principalmente en la forma de brotes epidémicos debidos a fuentes de agua contaminada, ya sea redes de agua potable, de superficie o recreativas. Los ooquistes de Cryptosporidium permanecen viables en agua de mar durante 1 año. También se ha documentado su concentración en moluscos bivalvos y existe evidencia creciente de que el parásito puede multiplicarse en ambientes libres de hospederos (Thompson et al., 2016).
Gracias a su pared gruesa, los ooquistes de Cryptosporidium resisten los tratamientos químicos usuales: no sufren alteración después de ser expuestos a 80 ppm de cloro/30 min, e incluso pueden tolerar 24 h en el cloro utilizado para blanqueado de ropa.
El empleo de ozono (1 ppm x 5 min), la congelación o calentamiento (>72° C durante 1 min ó 45 °C por 10 min después de iniciada la ebullición) son métodos más efectivos. Permanecen viables al cabo de una semana en la mayoría de los congeladores caseros. Debido a su tamaño, únicamente los filtros capaces de remover partículas de 1 µm resultan confiables.
Se considera una cloración adecuada del agua cuando se confirma una concentración de cloro residual de 0.5 mg/l (0.5 p.p.m).
Tratamiento.
Es necesario mantener el equilibrio hidroelectrolítico tanto en sujetos inmunocompetentes como inmunodeprimidos. En algunos pacientes es necesaria la alimentación parenteral. Fundamentalmente, el tratamiento consiste en medidas de sostén.
Los pacientes con SIDA deben iniciar/reiniciar el tratamiento con antirretrovirales.
Se sugiere tratamiento con nitazoxanida y de no ser posible, con paromomicina (UpToDate: This topic last updated: Oct 24, 2016).
Detección en agua.
Actualmente, la EPA (EEUU) y otras organizaciones de salud con metodología de vanguardia, utilizan la separación inmunomagnética para detección y aislamiento de protozoos en agua y la tinción con anticuerpos específicos fluorescentes. Otras técnicas que pueden ser utilizadas con el objetivo de purificación de quistes y ooquistes de protozoos incluyen gradientes de densidad, centrifugación de flujo, filtración continua de flujo, citometría de flujo. También se han desarrollado métodos moleculares, prometedores para la detección efectiva y simultánea de protozoos en agua, de acuerdo a varios autores, en comparación con los limitados resultados de la tinción convencional y microscopía, un punto de gran importancia en el campo de la salud pública. (Fletcher et al., 2012).
En México existe la legislación para regular los sistemas públicos operadores de agua para consumo. La NOM-127-SSA1-1994; NOM-179-SSA1-1998 incluye la determinación, en muestras de agua, de bacterias coliformes totales, E. coli, coliformes fecales, y la presencia de bacterias termotolerantes, como Citrobacter y Enterobacter. Los organismos deben estar ausentes. Tambien está publicado el Proyecto de Norma Oficial Mexicana PROY NOM-250-SSA1-2014 (DOF: 15/08/2014). Sin embargo, existe cierta confusión debido a los contenidos otro proyecto: Proyecto de Norma Oficial mexicana NOM-000-SSA1-2010. Y no existe la legislación clara para otros organismos, como los protozoos Cryptosporidium parvum y Giardia lamblia. (Olivas-Enríquez et al., 2013).
México. Límites máximos permisibles de microorganismos en agua |
||
Parámetro |
Unidad |
Límite máximo permisible |
Colifagos |
Fago/L |
Ausente/1 L |
E. coli o Coliformes fecales u organismos termotolerantes 1 |
NMP/100 mL |
<1,1 NMP/100 mL |
Giardia lamblia |
Quistes/L |
0/20 L |
1 Los métodos son excluyentes, las unidades de medida deberán reportarse de acuerdo a la metodología empleada. En: PROYECTO de Norma Oficial Mexicana NOM-000-SSA1-2010, Agua para uso y consumo humano. |
||
